胰十二指肠切除术后胰瘘风险预测模型的系统评价与Meta分析
DOI: 10.12449/JCH241121
Risk prediction models for pancreatic fistula after pancreaticoduodenectomy: A systematic review and a Meta-analysis
-
摘要:
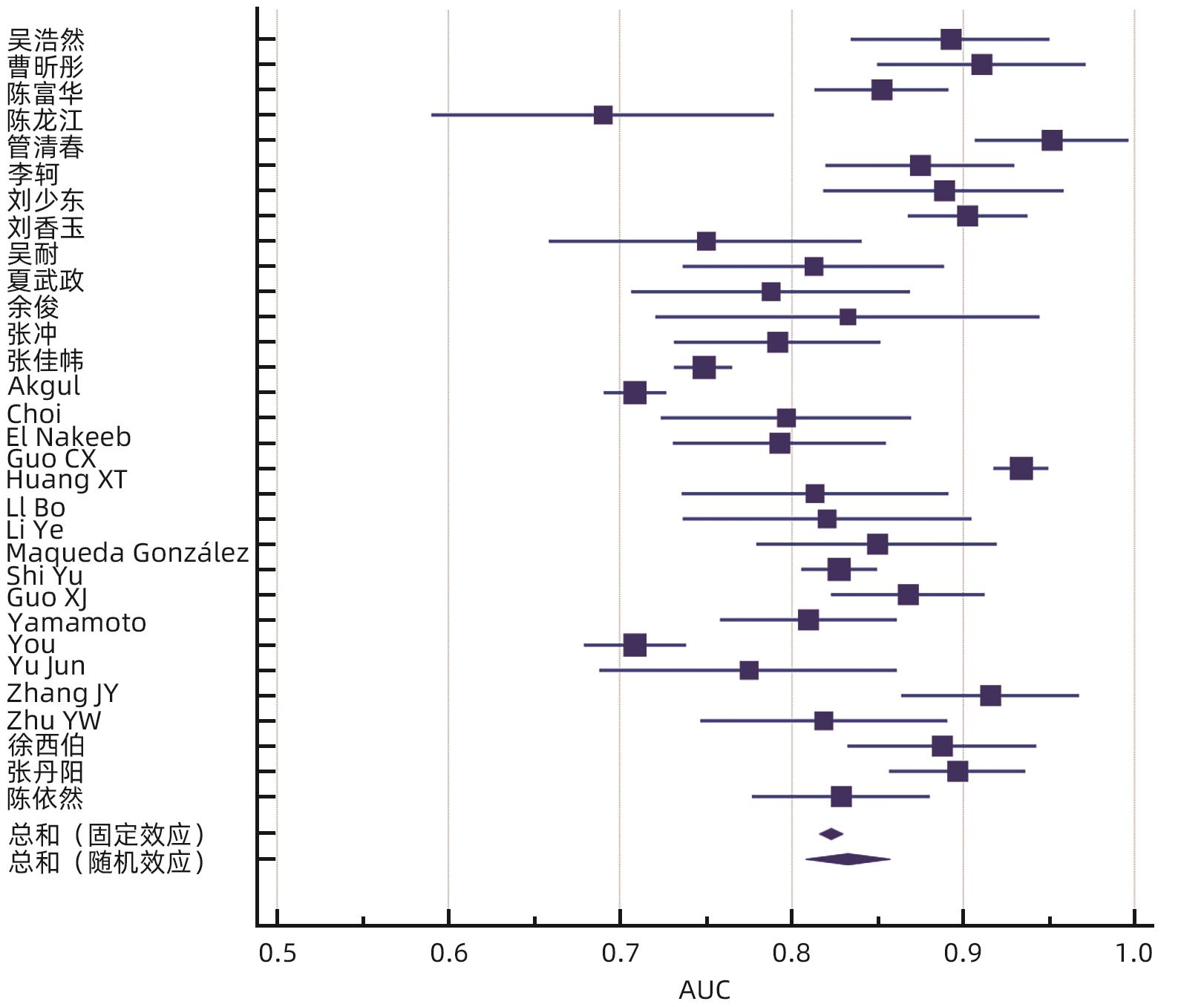
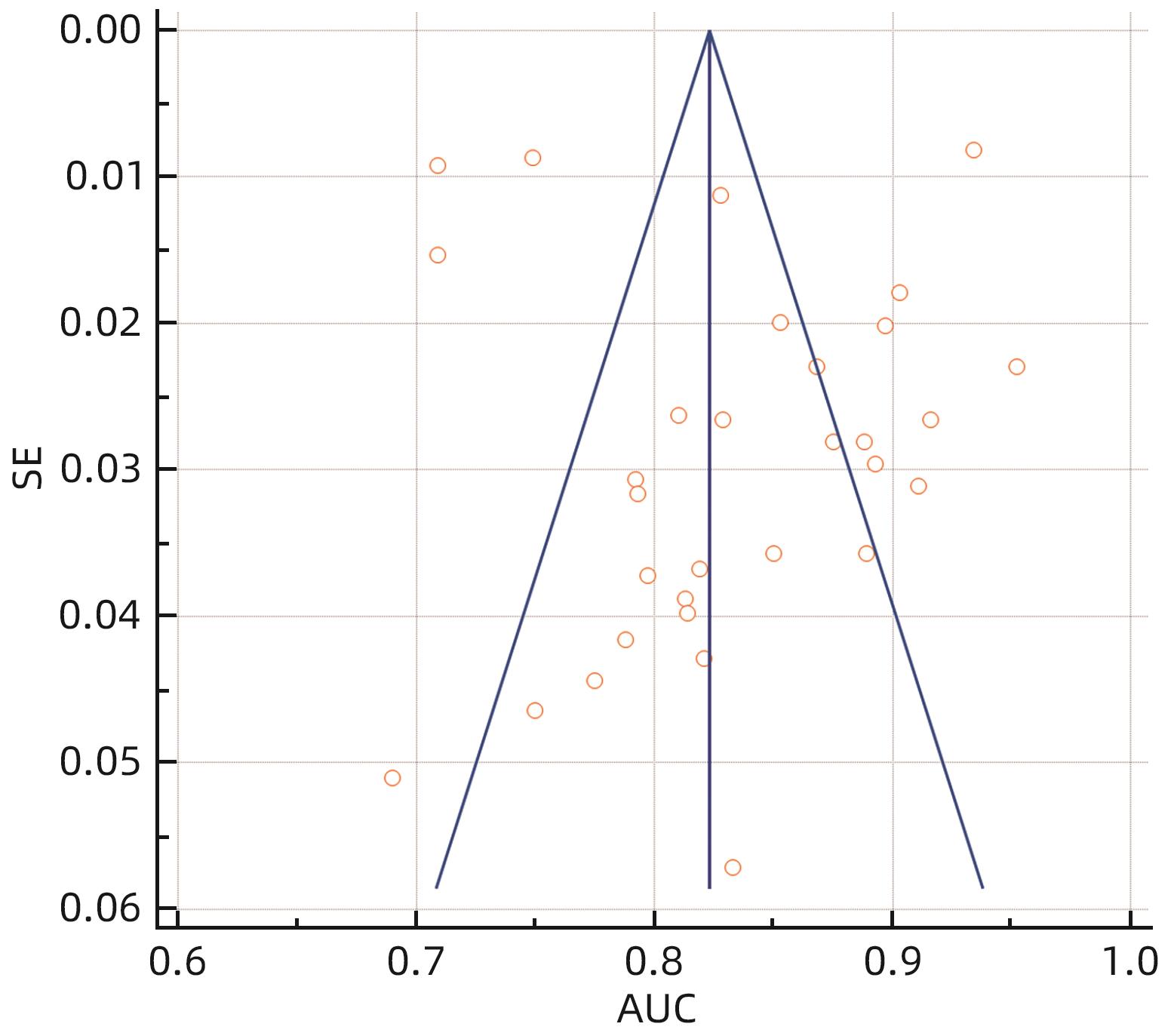
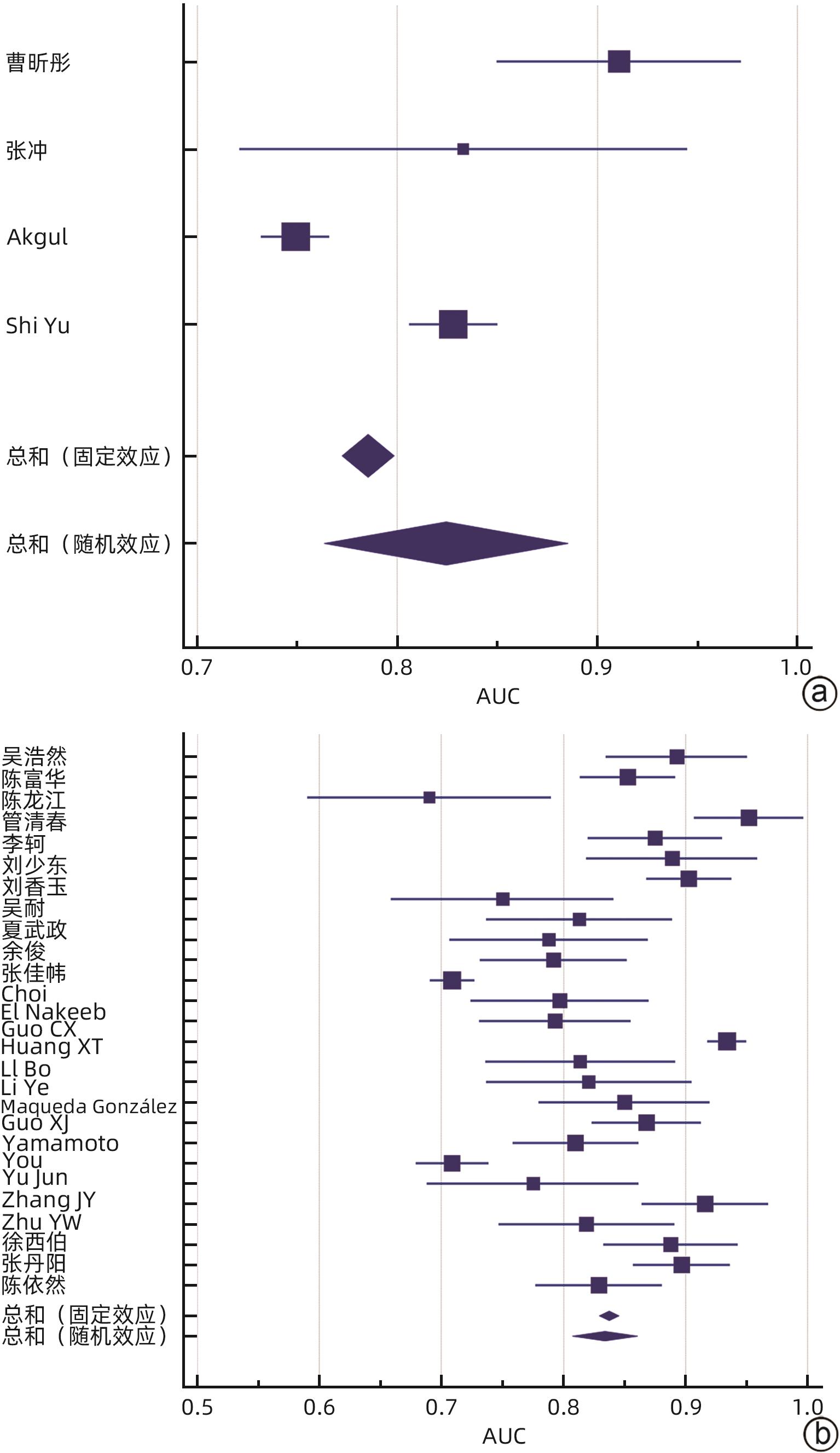
目的 系统评价胰十二指肠切除术后胰瘘(POPF)风险预测模型,为临床筛选应用POPF相关风险模型提供参考。 方法 本研究根据PRISMA指南完成,PROSPERO注册号:CRD42023437672。计算机检索PubMed、Scopus、Embase、Web of Science、Cochrane Library、中国知网、维普网、万方、中华医学期刊全文数据库和中国生物医学文献数据库公开发表的胰十二指肠切除POPF风险预测模型构建的研究文献,检索时限为建库至2024年4月26日。采用PROBAST工具评价文献质量,RevMan 5.4、MedCalc软件进行Meta分析。 结果 共纳入36篇文献、20 119例患者,胰十二指肠切除POPF发生率为7.4%~47.8%。36篇文献中,共构建55个风险预测模型,受试者工作特征曲线下面积(AUC)为0.690~0.952,其中52个模型AUC>0.7。文献质量评价结果均为高偏倚风险和适用性好。采用MedCalc软件对模型预测性能AUC进行统计学分析,合并的AUC为0.833(95%CI:0.808~0.857)。Meta分析显示:BMI、术后第1天引流液淀粉酶、术前血清白蛋白、胰管直径、胰腺质地、脂肪评分、肿瘤位置、失血量、性别、手术时间、主胰管指数、胰腺CT值是POPF的预测因子(P值均<0.05)。 结论 目前胰十二指肠切除POPF风险预测模型仍处于探索阶段,大部分预测模型的校准方法缺失,缺少外部验证,仅仅采用单因素分析筛选变量,偏倚风险较高,未来还需完善模型构建方法,以开发出预测准确度更高的风险预测模型。 Abstract:Objective To systematically review the risk prediction models for postoperative pancreatic fistula (POPF) after pancreaticoduodenectomy (PD), and to provide a reference for the clinical screening and application of POPF-related risk models. Methods This study was conducted according to the PRISMA guidelines, with a PROSPERO registration number of CRD42023437672. PubMed, Scopus, Embase, Web of Science, the Cochrane Library, CNKI, VIP, Wanfang Data, China Medical Journal Full-text Database, and CBM were searched for studies on establishing risk prediction models for POPF after PD published up to April 26, 2024. The PROBAST tool was used to assess the quality of articles, and RevMan 5.4 and MedCalc were used to perform the Meta-analysis. Results A total of 36 studies were included, involving 20 119 in total, and the incidence rate of POPF after PD was 7.4% — 47.8%. A total of 55 risk prediction models were established in the 36 articles, with an area under the receiver operating characteristic curve (AUC) of 0.690 — 0.952, among which 52 models had an AUC of >0.7. The quality assessment of the articles showed high risk of bias and good applicability. MedCalc was used to perform a statistical analysis of AUC values, and the results showed a pooled AUC of 0.833 (95% confidence interval: 0.808 — 0.857). The Meta-analysis showed that body mass index, amylase in drainage fluid on the first day after surgery, preoperative serum albumin, pancreatic duct diameter, pancreatic texture, fat score, tumor location, blood loss, sex, time of operation, main pancreatic duct index, and pancreatic CT value were predictive factors for POPF (all P<0.05). Conclusion The risk prediction models for POPF after PD is still in the exploratory stage. There is a lack of calibration methods and internal validation for most prediction models, and only the univariate analysis is used to for the screening of variables, which leads to the high risk of bias. In the future, it is necessary to improve the methods for model establishment, so as to develop risk prediction models with a higher prediction accuracy. -
注: 1,BMI;2,术后首日腹腔积液淀粉酶;3,术前血清白蛋白;4,性别;5,胰管直径;6,胰腺质地;7,失血量;8,脂肪评分;9,肿瘤位置;10,手术后第1天血清白蛋白;11,扩大淋巴清扫;12,高血压;13,非糖尿病;14,无腹部手术史;15,结肠前胃空肠吻合术;16,影像学胰管直径;17,年龄;18,病灶大小;19,胰脾比;20,血清肌酐;21,血清C反应蛋白;22,术后第3天中性粒细胞计数;23,体温;24,剩余胰腺体积;25,残端面积;26,萎缩评分;27,胰腺纤维化;28,胰腺指数;29,胰腺CT值;30,术中输血;31,腹腔引流液细菌培养结果;32,手术时间;33,胰管扩张;34,ASA评分;35,门静脉侵犯;36,主胰管指数;37,腹腔内脂肪厚度;38,甘油三酯;39,非胰腺疾病;40,术后高乳酸;41,手术部位感染;42,胃排空延迟;43,组织类型;44,诊断分类;45,腹内脂肪面积。
图 3 预测模型所纳入的预测因子
Figure 3. Predictors included in the prediction mode
表 1 纳入文献的基本特征及质量评价
Table 1. The basic characteristics and quality of the included literature were evaluated
第一作者 发表年份 国家 研究
类型
病变部位 平均年龄(模型/验证)(岁) 样本量
(模型/验证)(例)
胰瘘发生率(模型/验证)(%) PROBAST评价整体评估 偏倚风险 适用性 吴浩然[4] 2020 中国 回顾性 壶腹周围 58.6 176 7.4 高 好 Lee[5] 2024 韩国 回顾性 胰腺、十二指肠、胆总管、壶腹 63.4 881/452 47.8/31.8 高 好 曹昕彤[10] 2019 中国 前瞻性 胰腺和非胰腺 58 84 41.7 高 好 陈富华[11] 2020 中国 回顾性 胰腺、壶腹部 57.7±12.7 104 26.0 高 好 陈龙江[12] 2022 中国 回顾性 胰腺和非胰腺 58.61±12.67 106 33.9 高 好 管清春[13] 2020 中国 回顾性 胰腺和非胰腺 56.35±11.10 100 12 高 好 金继宽[14] 2019 中国 前瞻性 胰腺和非胰腺 57±5 388 7.99 高 好 李轲[15] 2020 中国 回顾性 胰腺和非胰腺 57.73±0.52 222/74 15.2 高 好 刘少东[16] 2020 中国 回顾性 胰腺和非胰腺 61.21±9.18 138 18.8 高 好 刘香玉[17] 2023 中国 回顾性 胰腺和非胰腺 60.4±8.7 441 15.6 高 好 吴耐[18] 2019 中国 回顾性 胰腺和非胰腺 60 161 17.4 高 好 夏武政[19] 2019 中国 回顾性 胰腺 - 225/136 17.8 高 好 余俊[20] 2024 中国 回顾性 胰腺和非胰腺 62±8 253/50 24.1/24.0 高 好 张冲[21] 2016 中国 前瞻性 胆管、十二指肠、胰腺 60.39±10.81 360/120 26.4/25.0 高 好 张佳帏[22] 2023 中国 回顾性 胰腺、壶腹部、十二指肠、胆总管 60±9 147 38.1 高 好 Akgul[23] 2019 美国 前瞻性 - 64 150/1 000 22 高 好 Choi[24] 2023 韩国 回顾性 壶腹周围 61.5±12.2 429 12.4 高 好 El Nakeeb[25] 2013 埃及 回顾性 壶腹、胰腺、十二指肠 52.58±10.82 471 7.7 高 好 Gu[26] 2023 中国 回顾性 - 64.8/65.6 3 609/1 347 16.7/16.6 高 好 Guo[27] 2020 中国 回顾性 - 62/65 220/78 22.7/15.4 高 好 Huang[28] 2021 中国 回顾性 - 59/66 762/420 11.4/6.2 高 好 Li[29] 2021 中国 回顾性 胰腺、壶腹 64.5 176 21.1 高 好 Li[30] 2019 中国 回顾性 胆管、胰腺、十二指肠、壶腹 62.1±10.1 170/122 20.2/21.1 高 好 Maqueda González[31] 2022 西班牙 回顾性 - 67 103 30.1 高 好 Shi[32] 2020 中国 前瞻性 - 59/60 718/272 15.6/13.2 高 好 Guo[33] 2019 中国 回顾性 胰头、十二指肠、胆管、壶腹 54.6 457/152 11.1 高 好 Yamamoto[34] 2011 日本 回顾性 壶腹周围 - 279/108 13.3/31.5 高 好 You[35] 2019 韩国 回顾性 胰腺和非胰腺 63 1 417/354 12.5 高 好 Yu[36] 2021 中国 回顾性 胰腺和非胰腺 60.9±8.7/61.3±6.8 124/99 25.8/23.2 高 好 Zhang[37] 2021 中国 回顾性 胰腺 - 232 18.2 高 好 Zhu[38] 2024 中国 回顾性 胰腺和非胰腺 - 200/232 16.0/18.2 高 好 徐西伯[39] 2020 中国 回顾性 壶腹周围 56±14 214/71 21.02 高 好 张子欢[40] 2023 中国 前瞻性 胰腺和非胰腺 63.5 227/151 12.43 高 好 张丹阳[41] 2024 中国 回顾性 胰头、十二指肠、胆总管、壶腹 - 257/108 29.96/29.63 高 好 周黎晨[42] 2023 中国 回顾性 胰头、十二指肠、胆总管 60/59 213/107 20.66/16.82 高 好 陈依然[43] 2016 中国 回顾性 胆管、胰腺、十二指肠 61±12 334/112 8.1 高 好 注:-,未明确指出。
表 2 预测模型建立情况
Table 2. The basic characteristics of the prediction model
第一作者 方法
筛选变量
建模数量 建模方法 EPV 缺失数据处理 AUC
(模型/验证)
校准方法 验证方法 吴浩然[4] 单因素分析 1 Logistic回归 2.605 未提及 0.893 Hosmer-Lemeshow 未提及 Lee[5] 单因素分析 4 Logistic回归 210.559 未提及 0.750/0.682 Calibration校正曲线 内部验证 曹昕彤[10] 单因素分析 1 Logistic回归 8.757 未提及 0.911 未提及 未提及 陈富华[11] 单因素分析 1 Logistic回归、列线图 6.800 已排除 0.853 Calibration校正曲线 内部验证 陈龙江[12] 单因素分析、LASSO回归 3 Logistic回归 17.967 未提及 0.69 未提及 未提及 管清春[13] 单因素分析 1 Logistic回归 3.000 未提及 0.952 未提及 未提及 金继宽[14] 单因素分析 1 Logistic回归 7.750 已排除 0.94 未提及 未提及 李轲[15] 单因素分析 1 Logistic回归、列线图 8.436 已排除 0.875/0.862 Hosmer-Lemeshow 内部验证 刘少东[16] 单因素分析 1 Logistic回归 8.648 已排除 0.889 未提及 未提及 刘香玉[17] 单因素分析 1 Logistic回归 22.932 已排除 0.903 Hosmer-Lemeshow 内部验证 吴耐[18] 单因素分析 1 Logistic回归 9.338 未提及 0.75 未提及 未提及 夏武政[19] 单因素分析 1 logistic回归 10.013 未提及 0.813/0.806 内部验证 余俊[20] 单因素分析 1 Logistic回归 20.324 已排除 0.788/0.804 Calibration校正曲线 内部验证 张冲[21] 单因素分析 1 Logistic回归 31.680 未提及 0.833/0.868 未提及 内部验证 张佳帏[22] 单因素分析 1 Logistic回归、列线图 18.669 已排除 0.729 Calibration校正曲线、决策曲线 内部验证 Akgul[23] 单因素分析 1 Logistic回归 8.250 未提及 0.710/0.698 Calibration校正曲线 外部验证 Choi[24] 单因素分析 1 Logistic回归、列线图 17.732 未提及 0.709/0.739 Calibration校正曲线 内部验证 El Nakeeb[25] 单因素分析 1 Logistic回归 18.133 未提及 0.797 未提及 未提及 Gu[26] 单因素分析、LASSO回归 5 Logistic回归、列线图 100.451 未提及 未提及/0.855 Calibration校正曲线Hosmer-Lemeshow、决策曲线 外部验证 Guo[27] 单因素分析 1 Logistic回归、列线图 12.485 未提及 0.793/0.816 Calibration校正曲线 内部验证 Huang[28] 单因素分析 1 Logistic回归、列线图 28.956 未提及 0.934/0.744 Calibration校正曲线、决策曲线 外部验证 Li[29] 单因素分析 1 Logistic回归、列线图 7.427 未提及 0.814 Calibration校正曲线 未提及 Li[30] 单因素分析 1 Logistic回归 8.585 未提及 0.821/0.845 未提及 内部验证 Maqueda González[31] 单因素分析 1 Logistic回归 10.334 未提及 0.85 未提及 未提及 Shi[32] 单因素分析、LASSO回归 1 Logistic回归 22.402 未提及 0.828/0.804 未提及 外部验证 Guo[33] 单因素分析 1 Logistic回归 16.909 未提及 0.868/0.887 未提及 外部验证 Yamamoto[34] 单因素分析 1 Logistic回归、列线图 7.421 未提及 0.808/0.834 未提及 内部验证 You[35] 单因素分析 1 Logistic回归、列线图 29.521 未提及 0.709/0.652 未提及 内部验证 Yu[36] 单因素分析 1 Logistic回归 7.998 已排除 0.775/0.848 Calibration校正曲线、决策曲线 内部验证 Zhang[37] 单因素分析 1 Logistic回归、列线图 8.445 未提及 0.916 未提及 未提及 Zhu[38] 单因素分析 1 Logistic回归 5.333 未提及 0.819/0.830 Calibration校正曲线 内部+外部 徐西伯[39] 单因素分析 1 Logistic回归 14.994 已排除 0.888/0.868 未提及 内部验证 张子欢[40] 单因素分析 11 Logistic回归、随机森林、SVM、决策树、KNN、GBM、LGBM、XGBoost、GNB、MNB和BNB 14.108 多重推断程序进行插补 0.72/0.70 未提及 内部验证 张丹阳[41] 单因素分析 1 Logistic回归、列线图 19.249 已排除 0.897/0.901 Calibration校正曲线 内部验证 周黎晨[42] 单因素分析 1 Logistic回归、列线图 14.669 已排除 0.869/0.881 Calibration校正曲线、决策曲线 内部验证 陈依然[43] 单因素分析 1 Logistic回归 13.527 未提及 0.829/0.885 未提及 内部验证 注:EPV,结局事件数与协变量个数比。
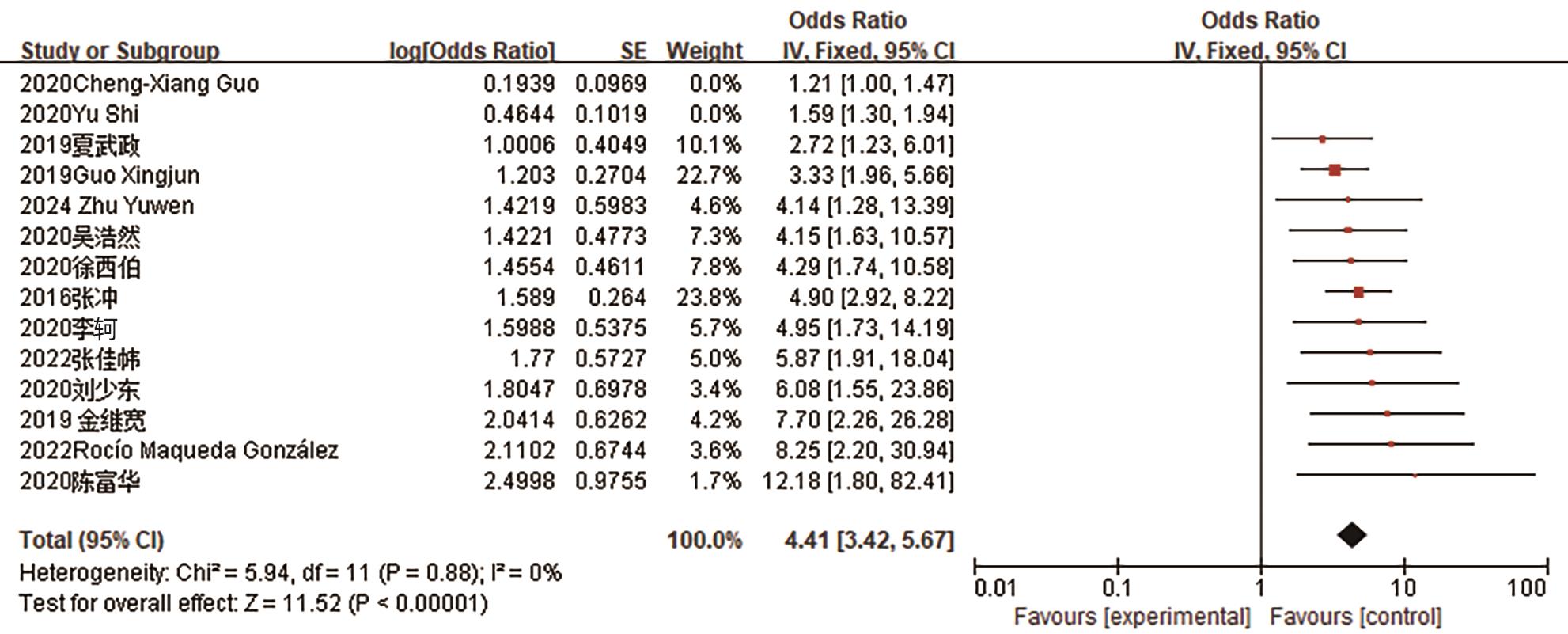
表 3 胰十二指肠切除POPF预测因子的Meta分析结果
Table 3. Meta analysis results of predictive factors for pancreatic fistula after pancreaticoduodenectomy
预测因子 纳入文献(篇) 异质性检验 效应模型 合并效应量 I2 值(%) P值 OR(95%CI) Z值 P值 BMI 11[12,17-18,21-22,26,28,35,38,42-43] 93 <0.000 01 随机效应 1.46(1.27~1.68) 5.26 <0.000 01 术后第1天引流淀粉酶 3[10,28-29] 97 <0.000 01 随机效应 1.42(1.10~1.83) 2.67 0.008 术前血清白蛋白≥35 g/L 3[10,30,35] 37 0.21 固定效应 0.89(0.83~0.96) 3.2 0.001 术前血清白蛋白<35 g/L 4[15,19,23,38] 0 0.67 固定效应 4.34 (2.48~7.57) 5.16 <0.000 01 胰管直径<3 mm 14[4,11,14-16,19,21-22,27,31-33,38-39] 82 <0.000 01 随机效应 3.61(2.46~5.30) 6.56 <0.000 01 胰管直径≥3 mm 12[5,13,18,23,25-26,28,30,35,41-43] 83 <0.000 01 随机效应 0.50(0.40~0.63) 6.11 <0.000 01 胰腺质地软 11[4,11,14-16,19,22,24,27,37,40] 44 0.05 随机效应 5.06(3.57~7.17) 9.12 <0.000 01 胰腺质地硬 7[13,18,23,26,30,41-42] 0 0.80 固定效应 0.18(0.15~0.21) 17.58 <0.000 01 脂肪评分 4[14,31-33] 50 0.11 随机效应 2.07(1.22~13.53) 12.69 0.007 肿瘤位置 8[5,13,20,22,24,34-36] 0 0.53 固定效应 2.25(1.79~2.81) 7.06 <0.000 01 失血量 4[11,15,30,38] 11 0.34 固定效应 5.49(3.15~9.59) 5.99 <0.000 01 性别 5[4-5,34-35,41] 50 0.09 随机效应 2.01(1.41~2.88) 3.82 0.000 1 手术时间 2[13-14] 0 0.45 固定效应 1.06(1.02~1.11) 2.65 0.008 主胰管指数 2[20,37] 0 >0.1 固定效应 0.00(0.00~0.01) 5.15 <0.000 01 胰腺CT值 2[20,36] 0 0.9 固定效应 0.94(0.90~0.98) 3.05 0.002 -
[1] KAWAIDA H, KONO H, HOSOMURA N, et al. Surgical techniques and postoperative management to prevent postoperative pancreatic fistula after pancreatic surgery[J]. World J Gastroenterol, 2019, 25( 28): 3722- 3737. DOI: 10.3748/wjg.v25.i28.3722. [2] SØREIDE K, LABORI KJ. Risk factors and preventive strategies for postoperative pancreatic fistula after pancreatic surgery: a comprehensive review[EB/OL].[ 2024-05-07]. https://www.tandfonline.com/doi/full/10.3109/00365521.2016.1169317. DOI: 10.3109/00365521.2016.1169317 [3] BASSI C, MARCHEGIANI G, DERVENIS C, et al. The 2016 update of the international study group(ISGPS) definition and grading of postoperative pancreatic fistula: 11 years after[J]. Surgery, 2017, 161( 3): 584- 591. DOI: 10.1016/j.surg.2016.11.014. [4] WU HR, ZHANG H, DUAN XH, et al. Complications after laparoscopic pancreaticoduodenectomy and establishment of predicting model for postoperative pancreatic fistula[J]. Chin J Gen Surg, 2020, 35( 11): 838- 842. DOI: 10.3760/cma.j.cn113855-20200211-00071.吴浩然, 张恒, 段小辉, 等. 腹腔镜胰十二指肠切除术后并发症发生的危险因素分析及术后胰瘘风险预测模型的建立[J]. 中华普通外科杂志, 2020, 35( 11): 838- 842. DOI: 10.3760/cma.j.cn113855-20200211-00071. [5] LEE W, PARK HJ, LEE HJ, et al. Deep learning-based prediction of post-pancreaticoduodenectomy pancreatic fistula[J]. Sci Rep, 2024, 14( 1): 5089. DOI: 10.1038/s41598-024-51777-2. [6] FUJII T, YAMADA S, MUROTANI K, et al. Oral food intake versus fasting on postoperative pancreatic fistula after distal pancreatectomy: A multi-institutional randomized controlled trial[J]. Medicine, 2015, 94( 52): e2398. DOI: 10.1097/MD.0000000000002398. [7] MOONS KGM, de GROOT JAH, BOUWMEESTER W, et al. Critical appraisal and data extraction for systematic reviews of prediction modelling studies: The CHARMS checklist[J]. PLoS Med, 2014, 11( 10): e1001744. DOI: 10.1371/journal.pmed.1001744. [8] WOLFF RF, MOONS KGM, RILEY RD, et al. PROBAST: A tool to assess the risk of bias and applicability of prediction model studies[J]. Ann Intern Med, 2019, 170( 1): 51- 58. DOI: 10.7326/M18-1376. [9] HANLEY JA, MCNEIL BJ. The meaning and use of the area under a receiver operating characteristic(ROC) curve[J]. Radiology, 1982, 143( 1): 29- 36. DOI: 10.1148/radiology.143.1.7063747. [10] CAO XT, SHEN DC, HUANG GW, et al. A single center prospective study of screening predictive factors and building predictive model for postoperative pancreatic fistula after pancreaticoduodenectomy[J]. Chin J Gen Surg, 2019, 28( 9): 1115- 1122. DOI: 10.7659/j.issn.1005-6947.2019.09.013.曹昕彤, 申鼎成, 黄耿文, 等. 胰十二指肠切除术后胰瘘的预测因素筛选及预测模型构建的单中心前瞻性研究[J]. 中国普通外科杂志, 2019, 28( 9): 1115- 1122. DOI: 10.7659/j.issn.1005-6947.2019.09.013. [11] CHEN FH. Prediction model of pancreatic fistula after laparoscopic pancreaticoduodenectomy with nomogram[D]. Fujian: Fujian Medical University, 2020.陈富华. 腹腔镜胰十二指肠切除术后胰瘘列线图预测模型[D]. 福建: 福建医科大学, 2020. [12] CHEN LJ, LI WB, TANG ZG, et al. The value of risk model based on CT radiomics in predicting postoperative pancreatic fistula following pancreaticoduodenectomy[J]. J Hepatopancreatobiliary Surg, 2022, 34( 11): 667- 673. DOI: 10.11952/j.issn.1007-1954.2022.11.007.陈龙江, 李微波, 汤志刚, 等. 基于CT影像组学胰十二指肠切除术后胰瘘风险预测模型及其价值[J]. 肝胆胰外科杂志, 2022, 34( 11): 667- 673. DOI: 10.11952/j.issn.1007-1954.2022.11.007. [13] GUAN QC. Risk factors and risk prediction of pancreatic fistula after laparoscopic pancreatoduodenectomy[D]. Changchun: Jilin University, 2020.管清春. 腹腔镜胰十二指肠切除术后胰瘘的危险因素分析及风险预测[D]. 长春: 吉林大学, 2020. [14] JIN JK. Study on risk factors and risk prediction of clinically relevant pancreatic fistula after laparoscopic pancreatoduodenectomy[D]. Wuhan: Huazhong University of Science and Technology, 2019.金继宽. 腹腔镜胰十二指肠切除术后临床相关性胰瘘危险因素及风险预测研究[D]. 武汉: 华中科技大学, 2019. [15] LI K. Screening of predictors of clinically relevant pancreatic fistula after pancreaticoduodenectomy and construction of predictive model[D]. Nanchang: Nanchang University, 2020.李轲. 胰十二指肠切除术后临床相关胰瘘预测因素的筛选与预测模型的构建[D]. 南昌: 南昌大学, 2020. [16] LIU SD. Risk factors analysis and risk prediction of pancreatic fistula after pancreatoduodenectomy[D]. Taiyuan: Shanxi Medical University, 2020.刘少东. 胰十二指肠切除术后胰瘘危险因素分析及风险预测[D]. 太原: 山西医科大学, 2020. [17] LIU XY, ZHENG C, CHEN X, et al. Development and validation of pancreatic fistula risk prediction model after laparoscopic pancreaticoduodenectomy[J]. Chin J Lab Diagn, 2023, 27( 2): 204- 209. DOI: 10.3969/j.issn.1007-4287.2023.02.021.刘香玉, 郑冲, 陈鑫, 等. 腹腔镜胰十二指肠根治术后胰瘘风险预测模型开发及验证[J]. 中国实验诊断学, 2023, 27( 2): 204- 209. DOI: 10.3969/j.issn.1007-4287.2023.02.021. [18] WU N, REN ZQ, ZHANG PB, et al. Risk factors and risk prediction of pancreatic fistula after pancreatoduodenectomy[J]. Anhui Med Pharm J, 2019, 23( 7): 1380- 1383. DOI: 10.3969/j.issn.1009-6469.2019.07.027.吴耐, 任泽强, 张蓬波, 等. 胰十二指肠切除术后胰瘘危险因素及风险预测[J]. 安徽医药, 2019, 23( 7): 1380- 1383. DOI: 10.3969/j.issn.1009-6469.2019.07.027. [19] XIA WZ. Establishment and clinical verification of risk assessment model of pancreatic fistula after pancreatoduodenectomy[D]. Guangzhou: Southern Medical University, 2019.夏武政. 胰十二指肠切除术后胰瘘风险评估模型的建立和临床验证[D]. 广州: 南方医科大学, 2019. [20] YU J, REN CY, CUI W, et al. Establishment of a risk prediction model for pancreatic fistula after pancreaticoduodenectomy: A study based on the 2016 edition of the definition and classification system of pancreatic fistula[J]. J Clin Hepatol, 2024, 40( 4): 773- 781. DOI: 10.12449/JCH240421.余俊, 任超逸, 崔巍, 等. 胰十二指肠切除术后胰瘘风险预测模型的建立: 基于2016新版胰瘘定义及分级系统[J]. 临床肝胆病杂志, 2024, 40( 4): 773- 781. DOI: 10.12449/JCH240421. [21] ZHANG C, ZHANG PB, ZHANG XZ, et al. Value of single factor combined with multi-factor risk screening model in risk prediction of pancreatic fistula after pancreaticoduodenectomy[J]. Shandong Med J, 2016, 56( 41): 56- 58. DOI: 10.3969/j.issn.1002-266X.2016.41.018.张冲, 张蓬波, 张秀忠, 等. 单因素联合多因素风险筛选模型在胰十二指肠切除术后胰瘘发生风险预测中的价值[J]. 山东医药, 2016, 56( 41): 56- 58. DOI: 10.3969/j.issn.1002-266X.2016.41.018. [22] ZHANG JW, HE CC, WANG CH. Construction and validation of a risk prediction model for pancreatic fistula after pancreaticoduodenectomy[J]. Chin J Endocr Surg, 2023, 17( 3): 268- 272. DOI: 10.3760/cma.j.cn.115807-20220104-00001.张佳帏, 贺宸宸, 王春晖. 胰十二指肠切除术后胰瘘风险预测模型的构建与验证[J]. 中华内分泌外科杂志, 2023, 17( 3): 268- 272. DOI: 10.3760/cma.j.cn.115807-20220104-00001. [23] AKGUL O, MERATH K, MEHTA R, et al. Postoperative pancreatic fistula following pancreaticoduodenectomy-stratification of patient risk[J]. J Gastrointest Surg, 2019, 23( 9): 1817- 1824. DOI: 10.1007/s11605-018-4045-x. [24] CHOI M, LEE JH, ROH YH, et al. Multidimensional nomogram to predict postoperative pancreatic fistula after minimally invasive pancreaticoduodenectomy[J]. Ann Surg Oncol, 2023, 30( 8): 5083- 5090. DOI: 10.1245/s10434-023-13360-3. [25] NAKEEB A EL, SALAH T, SULTAN A, et al. Pancreatic anastomotic leakage after pancreaticoduodenectomy. Risk factors, clinical predictors, and management(single center experience)[J]. World J Surg, 2013, 37( 6): 1405- 1418. DOI: 10.1007/s00268-013-1998-5. [26] GU ZT, DU YX, WANG P, et al. Development and validation of a novel nomogram to predict postoperative pancreatic fistula after pancreatoduodenectomy using lasso-logistic regression: An international multi-institutional observational study[J]. Int J Surg, 2023, 109( 12): 4027- 4040. DOI: 10.1097/JS9.0000000000000695. [27] GUO CX, SHEN YN, ZHANG Q, et al. Prediction of postoperative pancreatic fistula using a nomogram based on the updated definition[J]. Ann Surg Treat Res, 2020, 98( 2): 72- 81. DOI: 10.4174/astr.2020.98.2.72. [28] HUANG XT, HUANG CS, LIU C, et al. Development and validation of a new nomogram for predicting clinically relevant postoperative pancreatic fistula after pancreatoduodenectomy[J]. World J Surg, 2021, 45( 1): 261- 269. DOI: 10.1007/s00268-020-05773-y. [29] LI B, PU N, CHEN QD, et al. Comprehensive diagnostic nomogram for predicting clinically relevant postoperative pancreatic fistula after pancreatoduodenectomy[J]. Front Oncol, 2021, 11: 717087. DOI: 10.3389/fonc.2021.717087. [30] LI Y, ZHOU F, ZHU DM, et al. Novel risk scoring system for prediction of pancreatic fistula after pancreaticoduodenectomy[J]. World J Gastroenterol, 2019, 25( 21): 2650- 2664. DOI: 10.3748/wjg.v25.i21.2650. [31] MAQUEDA GONZÁLEZ R, DI MARTINO M, GALÁN GONZÁLEZ I, et al. Development of a prediction model of pancreatic fistula after duodenopancreatectomy and soft pancreas by assessing the preoperative image[J]. Langenbecks Arch Surg, 2022, 407( 6): 2363- 2372. DOI: 10.1007/s00423-022-02564-y. [32] SHI Y, GAO F, QI YF, et al. Computed tomography-adjusted fistula risk score for predicting clinically relevant postoperative pancreatic fistula after pancreatoduodenectomy: Training and external validation of model upgrade[J]. EBioMedicine, 2020, 62: 103096. DOI: 10.1016/j.ebiom.2020.103096. [33] GUO XJ, ZHU F, YANG MW, et al. A score model based on pancreatic steatosis and fibrosis and pancreatic duct diameter to predict postoperative pancreatic fistula after pancreatoduodenectomy[J]. BMC Surg, 2019, 19( 1): 75. DOI: 10.1186/s12893-019-0534-4. [34] YAMAMOTO Y, SAKAMOTO Y, NARA S, et al. A preoperative predictive scoring system for postoperative pancreatic fistula after pancreaticoduodenectomy[J]. World J Surg, 2011, 35( 12): 2747- 2755. DOI: 10.1007/s00268-011-1253-x. [35] YOU Y, HAN IW, CHOI DW, et al. Nomogram for predicting postoperative pancreatic fistula[J]. HPB(Oxford), 2019, 21( 11): 1436- 1445. DOI: 10.1016/j.hpb.2019.03.351. [36] YU J, REN CY, WANG J, et al. Establishment of risk prediction model of postoperative pancreatic fistula after pancreatoduodenectomy: 2016 edition of definition and grading system of pancreatic fistula: A single center experience with 223 cases[J]. World J Surg Oncol, 2021, 19( 1): 257. DOI: 10.1186/s12957-021-02372-6. [37] ZHANG JY, HUANG J, ZHAO SY, et al. Risk factors and a new prediction model for pancreatic fistula after pancreaticoduodenectomy[J]. Risk Manag Healthc Policy, 2021, 14: 1897- 1906. DOI: 10.2147/RMHP.S305332. [38] ZHU YW, WU D, YANG H, et al. Analysis of factors influencing pancreatic fistula after minimally invasive pancreaticoduodenectomy and establishment of a new prediction model for clinically relevant pancreatic fistula[J]. Surg Endosc, 2024, 38( 5): 2622- 2631. DOI: 10.1007/s00464-024-10770-6. [39] XU XB, JIA CP, JIA Y, et al. Construction and application value of prediction model of pancreatic fistula after pancreaticoduodenectomy[J]. Chin J Dig Surg, 2020, 19( 4): 408- 413. DOI: 10.3760/cma.j.cn115610-20200409-00240.徐西伯, 贾成朋, 贾勇, 等. 构建胰十二指肠切除术后胰瘘预测模型及其应用价值[J]. 中华消化外科杂志, 2020, 19( 4): 408- 413. DOI: 10.3760/cma.j.cn115610-20200409-00240. [40] ZHANG ZH. Research on risk factors and clinical prediction model of pancreatic fistula after pancreaticoduodenectomy based on machine learning[D]. Beijing: Peking Union Medical College, 2023.张子欢. 基于机器学习的胰十二指肠切除术发生胰瘘的危险因素及临床预测模型研究[D]. 北京: 北京协和医学院, 2023. [41] ZHANG DY, LEI P, ZHANG YB, et al. Construction and validation of a risk prediction model for clinically relevant pancreatic fistula after pancreaticoduodenectomy[J]. China J Gen Surg, 2024, 33( 3): 366- 375. DOI: 10.7659/j.issn.1005-6947.2024.03.007.张丹阳, 雷鹏, 张宇波, 等. 胰十二指肠切除术后临床相关胰瘘风险预测模型构建及验证[J]. 中国普通外科杂志, 2024, 33( 3): 366- 375. DOI: 10.7659/j.issn.1005-6947.2024.03.007. [42] ZHOU LC. Establishment and verification of prediction model of pancreatic fistula after pancreatoduodenectomy[D]. Luzhou: Southwest Medical University, 2023.周黎晨. 胰十二指肠切除术后胰瘘预测模型建立与验证[D]. 泸州: 西南医科大学, 2023. [43] CHEN YR, TIAN XD, XIE XH, et al. Risk factors of postoperative pancreatic fistula after pancreaticoduodenectomy and its predictive score[J]. Chin J Surg, 2016, 54( 1): 39- 43. DOI: 10.3760/cma.j.issn.0529-5815.2016.01.010.陈依然, 田孝东, 谢学海, 等. 胰十二指肠切除术后胰瘘风险预测系统的建立和应用[J]. 中华外科杂志, 2016, 54( 1): 39- 43. DOI: 10.3760/cma.j.issn.0529-5815.2016.01.010. [44] GROUP PS, COMMITTEE W, PANDE R, et al. External validation of postoperative pancreatic fistula prediction scores in pancreatoduodenectomy: A systematic review and meta-analysis[J]. HPB(Oxford), 2022, 24( 3): 287- 298. DOI: 10.1016/j.hpb.2021.10.006. [45] van der PLOEG T, AUSTIN PC, STEYERBERG EW. Modern modelling techniques are data hungry: A simulation study for predicting dichotomous endpoints[J]. BMC Med Res Methodol, 2014, 14: 137. DOI: 10.1186/1471-2288-14-137. [46] CHEN XP, ZHANG Y, ZHUANG YY, et al. PROBAST: A tool for assessing risk of bias in the study of diagnostic or prognostic multi-factorial predictive models[J]. Chin J Evid Based Med, 2020, 20( 6): 737- 744. DOI: 10.7507/1672-2531.201910087.陈香萍, 张奕, 庄一渝, 等. PROBAST: 诊断或预后多因素预测模型研究偏倚风险的评估工具[J]. 中国循证医学杂志, 2020, 20( 6): 737- 744. DOI: 10.7507/1672-2531.201910087. [47] RANALLI MG, SALVATI N, PETRELLA L, et al. M-quantile regression shrinkage and selection via the Lasso and Elastic Net to assess the effect of meteorology and traffic on air quality[J]. Biom J, 2023, 65( 8): e2100355. DOI: 10.1002/bimj.202100355. [48] ZHANG Q, YUAN KH, WANG LJ. Asymptotic bias of normal-distribution-based maximum likelihood estimates of moderation effects with data missing at random[J]. Br J Math Stat Psychol, 2019, 72( 2): 334- 354. DOI: 10.1111/bmsp.12151. [49] ZHOU CY, YAO LB. Biochemistry and molecular biology[M]. 9th ed. Beijing: People’s Medical Publishing House, 2018: 350- 351.周春燕, 药立波. 生物化学与分子生物学[M]. 9版. 北京: 人民卫生出版社, 2018: 350- 351. [50] SLEEP D. Albumin and its application in drug delivery[J]. Expert Opin Drug Deliv, 2015, 12( 5): 793- 812. DOI: 10.1517/17425247.2015.993313. [51] YANG JX, YE SY, DAI D. Risk factors and preventive measures for postoperative pancreatic fistula after pancreaticoduodenectomy[J]. World Chin J Dig, 2020, 28( 18): 914- 919. DOI: 10.11569/wcjd.v28.i18.914.杨均兴, 叶思严, 戴东. 胰十二指肠切除术后胰瘘的相关危险因素及预防措施的最新进展[J]. 世界华人消化杂志, 2020, 28( 18): 914- 919. DOI: 10.11569/wcjd.v28.i18.914. [52] WANG XL, TU YY, WANG W, et al. Risk factors for pancreatic fistula after pancreaticoduodenectomy[J]. J Clin Hepatol, 2017, 33( 1): 116- 120. DOI: 10.3969/j.issn.1001-5256.2017.01.025.王小龙, 涂彦渊, 王巍, 等. 胰十二指肠切除术后胰瘘发生的危险因素分析[J]. 临床肝胆病杂志, 2017, 33( 1): 116- 120. DOI: 10.3969/j.issn.1001-5256.2017.01.025. [53] Chinese Society of Endoscopy, Chinese Medical Association; Endoscopic Physician Branch of Chinese Medical Doctor Association; Beijing Society of Digestive Endoscopy, Beijing Medical Association. Chinese expert consensus on the endoscopic diagnosis and treatment of pancreatic fistula(2020, Beijing)[J]. J Clin Hepatol, 2021, 37( 4): 803- 808. DOI: 10.3969/j.issn.1001-5256.2021.04.016.中华医学会消化内镜学分会, 中国医师协会内镜医师分会, 北京医学会消化内镜学分会. 中国胰瘘消化内镜诊治专家共识(2020, 北京)[J]. 临床肝胆病杂志, 2021, 37( 4): 803- 808. DOI: 10.3969/j.issn.1001-5256.2021.04.016. [54] HE CC, WANG CH, TANG YF. Research status of abdominal drainage after pancreaticoduodenectomy[J]. Chin J Med Offic, 2022, 50( 1): 99- 101, 105. DOI: 10.16680/j.1671-3826.2022.01.31.贺宸宸, 王春晖, 唐裕福. 胰十二指肠切除术后腹腔引流研究现状[J]. 临床军医杂志, 2022, 50( 1): 99- 101, 105. DOI: 10.16680/j.1671-3826.2022.01.31. [55] HALLE-SMITH JM, VINUELA E, BROWN RM, et al. A comparative study of risk factors for pancreatic fistula after pancreatoduodenectomy or distal pancreatectomy[J]. HPB(Oxford), 2017, 19( 8): 727- 734. DOI: 10.1016/j.hpb.2017.04.013. [56] RILEY RD, ENSOR J, SNELL KIE, et al. Calculating the sample size required for developing a clinical prediction model[J]. BMJ, 2020, 368: m441. DOI: 10.1136/bmj.m441. -


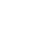 PDF下载 ( 2569 KB)
PDF下载 ( 2569 KB)

 下载:
下载: